Coronavac atinge 78% de eficácia em testes no Brasil, segundo o Governo de São Paulo
Estudos comprovaram que a vacina do Butantan tem eficácia de 100% para casos graves e moderados, afirma a gestão estadual. Pedido emergencial deve ser oficializado até esta sexta
BEATRIZ JUCÁ
07 JAN 2021 - São Paulo
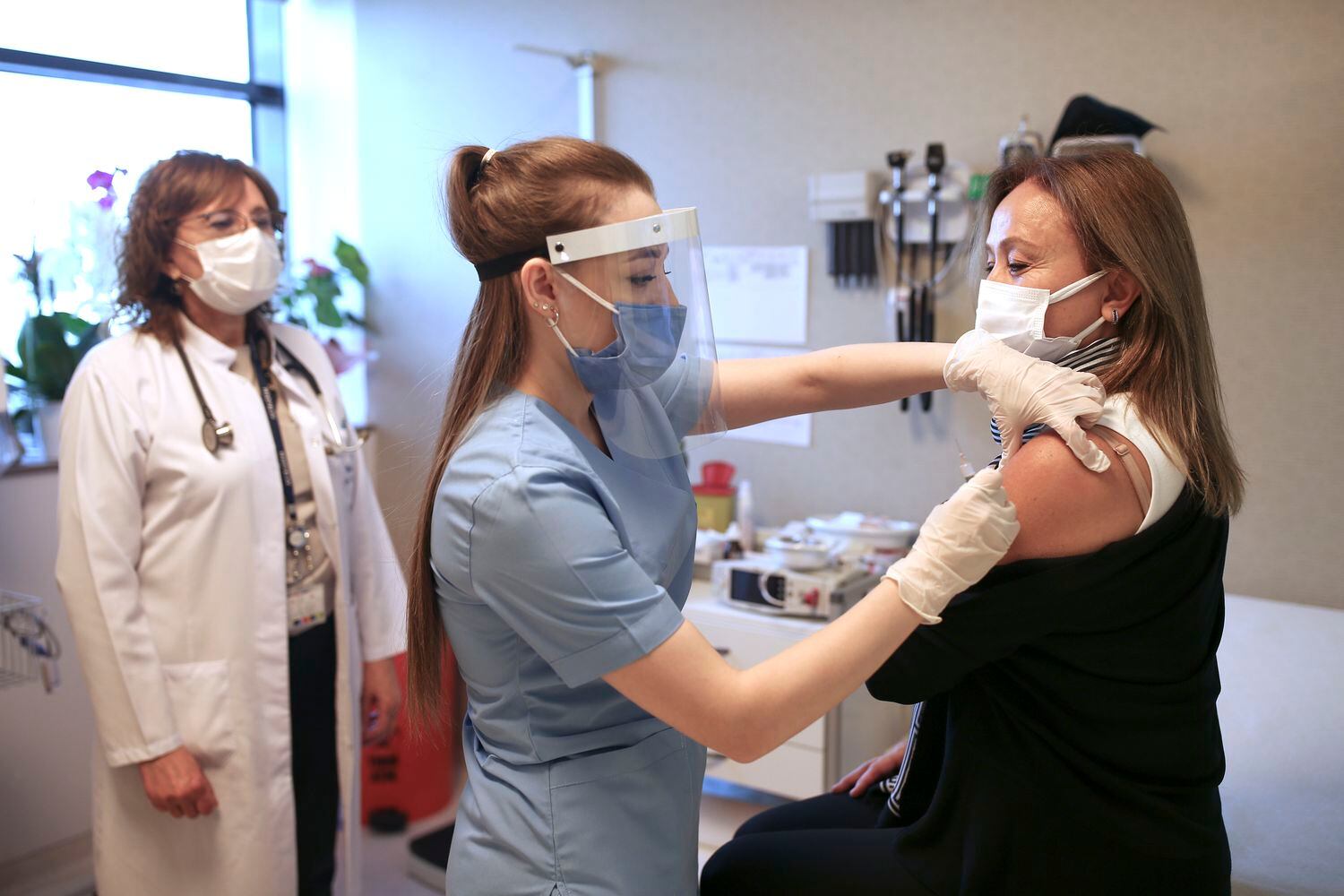
Uma voluntária participa dos testes da Coronavac em Istambul.EMRAH GUREL / AP
A Coronavac, vacina desenvolvida pelo laboratório chinês Sinovac em conjunto com o Instituto Butantan, apresentou 78% de eficácia contra a covid-19 no ensaio desenvolvido no Brasil e patrocinado pelo Governo de São Paulo, segundo as autoridades de saúde do Estado. O imunizante, alçado ao centro da disputa política entre o presidente Jair Bolsonaro e o governador João Doria, também foi capaz de garantir proteção total contra mortes nos voluntários vacinados que contraíram a doença, conforme já vinha destacando o Governo paulista. As informações foram repassadas pela gestão estadual, que divulgou os percentuais sem dar maiores detalhes sobre os dados numéricos da pesquisa. Um relatório só deve ser apresentado após o pedido para uso emergencial do medicamento na Anvisa, que já foi iniciado nesta quinta-feira (7) e que deve ser apresentado formalmente até a sexta-feira (8). O Governo de São Paulo espera começar a vacinar os grupos prioritários ―que inclui idosos, profissionais da saúde, indígenas e quilombolas― no dia 25 de janeiro. A estimativa de Doria é de chegar a 9 milhões de pessoas vacinadas até março.
Desde o mês de julho, 12.476 profissionais de saúde da linha de frente da covid-19, mais suscetíveis a contrair a infecção, participaram dos testes. O estudo foi realizado com 16 centros clínicos em oito estados brasileiros e acompanhado por organismos internacionais de saúde. O presidente do Butantan, Dimas Covas, explicou que internação hospitalar, casos graves e casos moderados foram evitados em 100% das análises de imunizados. E que 78% dos vacinados não precisaram de atendimento ambulatorial, quando a pessoa tem um sintoma importante que necessita de assistência médica. “Estamos evitando casos graves, moderados e reduzindo as manifestações mais leves. Então é uma excelente vacina até o momento. Precisamos que ela chegue ao braço das pessoas o mais rapidamente possível”, afirma.
O rito na Anvisa para solicitar o uso emergencial, segundo o presidente do Butantan, prevê uma reunião inicial que já foi realizada na manhã desta terça-feira, quando representantes dos dois órgãos estiveram em reunião para apresentação do estudo brasileiro. Uma nova reunião para esclarecimentos à agência está marcada para o final do dia, e o Butantan espera fazer o pedido emergencial oficialmente até a sexta-feira. Só após esta formalização, deverá divulgar o relatório do estudo, com dados mais específicos sobre os grupos. Por enquanto, o que Dimas Covas adiantou é que metade dos voluntários recebeu a vacina e a outra metade o placebo. E que não houve diferença de eficácia observada entre jovens e idosos. “Não há neste momento diferenças observadas”, pontua. Como se sabe que idosos têm uma imunologia diferente de grupos mais jovens, o instituto segue estudos com voluntários idosos para analisar se é necessário uma terceira dose e qual o intervalo entre elas é o mais adequado para esta população.
Em novembro, o ensaio da fase 3 já havia atingido o número mínimo de voluntários infectados no Brasil para a apresentação de resultados preliminares, superando os 151 infectados necessários às conclusões ― o que supõe mais robustez aos resultados. Estes dados preliminares seriam apresentados inicialmente no dia 12 de dezembro, mas a partir daí houve vários adiamentos para a apresentação das informações. Primeiro, o Governo de São Paulo mudou de estratégia e disse que apresentaria dados mais consolidados para pedir o registro definitivo e não mais a autorização para uso emergencial à Anvisa. Nos dias seguintes, porém, voltou atrás e disse que solicitaria as duas autorizações. A expectativa era de apresentação dos resultados de eficácia no último dia 23 de dezembro, mas o Butantan adiou novamente a apresentação alegando uma cláusula contratual para apresentação unificada de dados de diferentes países. Nas últimas semanas, porém, as autoridades vinham repetindo que o imunizante havia demonstrado eficácia e segurança. Um pedido de registro definitivo, porém, só deve ser feito após a unificação de dados de vários países e pela própria Sinovac.
O Governo de São Paulo espera ter o aval da agência para iniciar a vacinação de forma emergencial no dia 25 de janeiro. A estratégia estadual inclui converter espaços além dos postos tradicionais ―como escolas, estações de trem, farmácias e implementar também um drive thru― em pontos de vacinação. A ideia é vacinar 9 milhões de pessoas em três meses. Para completar toda a primeira fase, são necessárias 18 milhões de doses. O Governo também diz já ter adquirido seringas e estima que serão necessárias 27 milhões delas nesta fase. Até o momento, cerca de 10,8 milhões de doses da Coronavac chegaram ao país.

Apresentação enviada pelo Governo de São Paulo.DIVULGAÇÃO
Mas pesa sobre este planejamento estadual os desdobramentos do plano nacional de vacinação. Sob pressão de governadores e em meio à disputa política entre Doria e Bolsonaro, o Governo Federal agora corre contra o tempo para conseguir começar a imunização antes de São Paulo. Um dia antes do anúncio dos dados da Coronavac, o ministro da Saúde, Eduardo Pazuello, foi à televisão prometer o início da imunização para janeiro. Falou em uma previsão de 354 milhões de doses para 2021, contando com 100 milhões de doses da Coronavac por meio de um memorando de entendimentos firmado com o Instituto Butantan. Pazuello não detalhou quando exatamente as vacinas estariam disponíveis, mas nos últimos dias tem negociado a aquisição de 2 milhões de doses da Astrazeneca para antecipar a vacinação. O ministro também anunciou uma Medida Provisória assinada pelo presidente para garantir a compra de vacinas mesmo antes de receber a aprovação da Anvisa, um argumento repetido pelas autoridades de saúde federais para justificar a demora nas negociações.
Negociações para exportar a vacina
Paralelamente, o Instituto Butantan negocia uma futura exportação da Coronavac. Dimas Covas afirma que pelo menos seis países já iniciaram conversas neste sentido, como Argentina, Peru, Bolívia, Uruguai, Honduras e Equador. “Essas negociações dependem do contrato para prever a data de fornecimento. Neste momento, não temos nenhum contrato finalizado ainda”, salientou.
Também influi nesta questão as tratativas com o Governo Federal, em meio à disputa política entre Doria e Bolsonaro pelos louros de iniciar uma campanha. Em vários momentos durante a coletiva de imprensa para apresentação de dados da Coronavac, o governador de São Paulo criticou aqueles que consideraram a covid-19 uma “gripezinha”, tentou marcar seu posto do lado da ciência e contra o negacionismo e pediu publicamente que a Anvisa não ceda a possíveis pressões que possam atrasar a autorização emergencial da Coronavac. “Que em nenhum momento pense em atender a qualquer pressão de ordem ideológica ou qualquer outro tipo de pressão para prejudicar a velocidade interativa de oferecer esta vacina”, declarou.
Fonte: El País
Comentários
Postar um comentário
Todas postagem é previamente analisada antes de ser publicada.