Estudo da vacina de Oxford é paralisado após suposta reação adversa
AstraZeneca decide interromper seus testes de fase final no mundo, enquanto investiga possível efeito colateral grave em voluntário. Pazuello disse que vacina estaria disponível no Brasil já em janeiro.
DW
09.09.2020
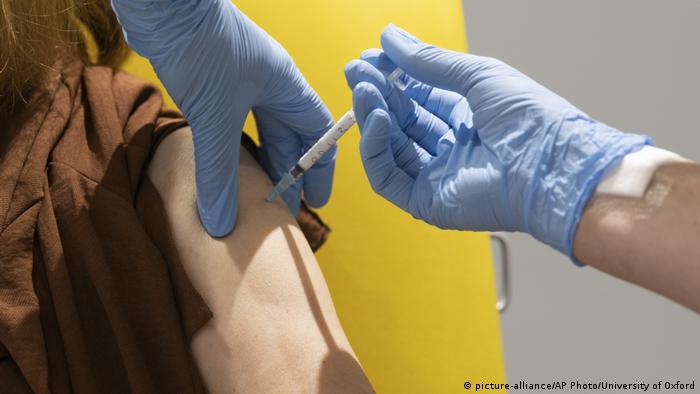
A fase final dos testes da vacina é realizada também no Brasil, em parceria com a Fiocruz
A farmacêutica AstraZeneca informou nesta terça-feira (08/09) que interrompeu o estudo de sua vacina contra a covid-19, desenvolvida em parceria com a Universidade de Oxford, enquanto investiga um possível efeito colateral grave em um paciente.
A fase final dos testes da vacina, uma das candidatas mais promissoras do mundo, é realizada também no Brasil, em parceria com a Fundação Oswaldo Cruz (Fiocruz).
"Como parte dos testes globais controlados e randomizados em andamento da vacina de Oxford contra o coronavírus, nosso processo de revisão padrão foi acionado e voluntariamente paralisamos a vacinação para permitir a revisão dos dados de segurança por um comitê independente", comunicou a AstraZeneca.
A empresa não deu detalhes sobre a suposta reação adversa, chamando-a apenas de "doença possivelmente inexplicada". A farmacêutica deverá agora apurar se o efeito colateral observado no voluntário tem, de fato, alguma relação com a vacina.
O site de notícias Stat, especializado em saúde e tecnologia, foi quem primeiro noticiou a interrupção nos testes, afirmando que o incidente ocorrera com um paciente no Reino Unido.
Segundo o jornal americano The New York Times, o paciente que apresentou um possível efeito colateral grave recebeu o diagnóstico de mielite transversa, uma síndrome inflamatória que afeta a medula espinhal e é frequentemente provocada por infecções virais.
O porta-voz da AstraZeneca, que mais tarde confirmou a paralisação, disse que a vacinação será interrompida nos Estados Unidos e nos demais países participantes.
No mês passado, a empresa começou a recrutar 30 mil pessoas nos EUA, em seu mais abrangente estudo da vacina. Milhares de pessoas estão sendo testadas também no Reino Unido, enquanto projetos menores são realizados no Brasil e na África no Sul.
Suspensões temporárias de grandes estudos médicos não são incomuns, e investigar qualquer reação grave ou inesperada é parte obrigatória dos testes de segurança. A AstraZeneca apontou ser possível que o problema tenha sido uma coincidência, já que doenças de todos os tipos podem surgir em estudos que envolvem milhares de pessoas.
"Estamos trabalhando para agilizar a revisão do evento único para minimizar qualquer potencial impacto no cronograma de testes", comunicou a empresa.
O anúncio ocorreu no mesmo dia em que a AstraZeneca e outras oito farmacêuticas se comprometeram, de forma conjunta e pouco usual, a defender os mais altos padrões éticos e científicos no desenvolvimento de suas vacinas contra a covid-19. Entre as demais signatárias estão Pfizer, Johnson & Johnson, Merck, Moderna, Sanofi e Biontech.
O anúncio também vem no mesmo dia em que o ministro interino da Saúde, Eduardo Pazuello, declarou que a vacinação no país terá início já em janeiro de 2021.
"Estamos fazendo os contratos com quem fabrica a vacina, e a previsão é de que essa vacina chegue para nós a partir de janeiro. Em janeiro do ano que vem, começamos a vacinar todo mundo", declarou ele, em reunião ministerial.
A vacina em questão é justamente a desenvolvida pela AstraZeneca e a Universidade de Oxford, que só receberá autorização para ser usada na população quando os estudos forem concluídos e comprovarem sua eficácia e segurança.
Fonte: DW
Comentários
Postar um comentário
Todas postagem é previamente analisada antes de ser publicada.